El dia martes vimos los enlaces quimicos de oxidos metalicos comprobando su conductividad, su ph y su reaccion con el calor tanto humedos como secos, comprobando que no todos los metales tienen conductividad.
el dia jueves vimos los oxidos no metalicos, su conductividad y ph de los acidos, al igual que las reacciones de los acidos y metales en agua e indicador universal...
viernes, 19 de noviembre de 2010
PUENTES DE HIDROGENO
l puente de hidrógeno es un enlace que se establece entre moléculas capaces de generar cargas parciales. El agua, es la sustancia en donde los puentes de hidrógeno son más efectivos, en su molécula, los electrones que intervienen en sus enlaces, están más cerca del oxígeno que de los hidrógenos y por esto se generan dos cargas parciales negativas en el extremo donde está el oxígeno y dos cargas parciales positivas en el extremo donde se encuentran los hidrógenos. La presencia de cargas parciales positivas y negativas hace que las moléculas de agua se comporten como imanes en los que las partes con carga parcial positiva atraen a las partes con cargas parciales negativas. De tal suerte que una sola molécula de agua puede unirse a otras 4 moléculas de agua a través de 4 puentes de hidrógeno. Esta característica es la que hace al agua un líquido muy especial.

Los puentes de Hidrógeno, se forman por átomos de Hidrógeno localizados entre átomos electronegativos. Cuando un átomo de Hidrógeno está unido covalentemente, a una átomo electronegativo, ej. Oxígeno o Nitrógeno, asume una densidad (d) de carga positiva, debido a la elevada electronegatividad del átomo vecino. Esta deficiencia parcial en electrones, hace a los átomos de Hidrógeno susceptibles de atracción por los electrones no compartidos en los átomos de Oxígeno o Nitrógeno
Obsérvese la configuración electrónica del Oxígeno:
8O 1s2 2s2 2pxêé pyé pzé
de ahí que :
:
 :
: d+ d+
d-
TABLA PERIODICA
La tabla periódica de los elementos clasifica, organiza y distribuye los distintos elementos químicos, conforme a sus propiedades y características.
Suele atribuirse la tabla a Dimitri Mendeleiev, quien ordenó los elementos basándose en la variación manual de las propiedades químicas, si bien Julius Lothar Meyer, trabajando por separado, llevó a cabo un ordenamiento a partir de las propiedades físicas de los átomos. La forma actual es una versión modificada de la de Mendeliev, fue diseñada por Alfred Werner.
Suele atribuirse la tabla a Dimitri Mendeleiev, quien ordenó los elementos basándose en la variación manual de las propiedades químicas, si bien Julius Lothar Meyer, trabajando por separado, llevó a cabo un ordenamiento a partir de las propiedades físicas de los átomos. La forma actual es una versión modificada de la de Mendeliev, fue diseñada por Alfred Werner.
OXIDOS NO METALICOS
No metales se denomina a los elementos químicos que no son metales. Los no metales, excepto el hidrógeno, están situados en la tabla periódica de los elementos en el bloque p. Los elementos de este bloque son no-metales, excepto los metaloides (B, Si, Ge, As, Sb, Te), todos los gases nobles (He, Ne, Ar, Kr, Xe, Rn), y algunos metales (Al, Ga,In, Tl, Sn, Pb).
En orden de número atómico:
El hidrógeno normalmente se sitúa encima de los metales alcalinos, pero normalmente se comporta como un no metal. Un no metal suele ser aislante o semiconductor de la electricidad. Los no metales suelen formar enlaces iónicos con los metales, ganando electrones, o enlaces covalentes con otros no metales, compartiendo electrones. Sus óxidos son ácidos.
Los no metales forman la mayor parte de la tierra, especialmente las capas más externas, y los organismos están compuestos en su mayor parte por no metales. Algunos no metales, en condiciones normales, son diatómicos en el estado elemental: hidrógeno (H2), nitrógeno (N2), oxígeno (O2), flúor (F2), cloro (Cl2), bromo (Br2) y yodo (I2). Los no metales varían mucho en su apariencia no son lustrosos y por lo general son malos conductores del calor y la electricidad. Sus puntos de fusión son más bajos que los de los metales (aunque el diamante, una forma de carbono, se funde a 3570 ºC). Varios no metales existen en condiciones ordinarias como moléculas diatómicas. En esta lista están incluidos cinco gases (H2, N2, 02, F2 y C12), un líquido (Br2) y un sólido volátil (I2). El resto de los no metales son sólidos que pueden ser duros como el diamante o blandos como el azufre. Al contrario de los metales, son muy frágiles y no pueden estirarse en hilos ni en láminas. Se encuentran en los tres estados de la materia a temperatura ambiente: son gases (como el oxígeno), líquidos (bromo) y sólidos (como el carbono). No tienen brillo metálico y no reflejan la luz. Muchos no metales se encuentran en todos los seres vivos: carbono, hidrógeno, oxígeno, nitrógeno, fósforo y azufre en cantidades importantes. Otros son oligoelementos: flúor, silicio, arsénico, yodo, cloro.
En orden de número atómico:
- Hidrógeno (H)
- Carbono (C)
- Nitrógeno (N)
- Oxígeno (O)
- Flúor (F)
- Fósforo (P)
- Azufre (S)
- Cloro (Cl)
- Selenio (Se)
- Bromo (Br)
- Yodo (I)
- Astato (At)
El hidrógeno normalmente se sitúa encima de los metales alcalinos, pero normalmente se comporta como un no metal. Un no metal suele ser aislante o semiconductor de la electricidad. Los no metales suelen formar enlaces iónicos con los metales, ganando electrones, o enlaces covalentes con otros no metales, compartiendo electrones. Sus óxidos son ácidos.
Los no metales forman la mayor parte de la tierra, especialmente las capas más externas, y los organismos están compuestos en su mayor parte por no metales. Algunos no metales, en condiciones normales, son diatómicos en el estado elemental: hidrógeno (H2), nitrógeno (N2), oxígeno (O2), flúor (F2), cloro (Cl2), bromo (Br2) y yodo (I2). Los no metales varían mucho en su apariencia no son lustrosos y por lo general son malos conductores del calor y la electricidad. Sus puntos de fusión son más bajos que los de los metales (aunque el diamante, una forma de carbono, se funde a 3570 ºC). Varios no metales existen en condiciones ordinarias como moléculas diatómicas. En esta lista están incluidos cinco gases (H2, N2, 02, F2 y C12), un líquido (Br2) y un sólido volátil (I2). El resto de los no metales son sólidos que pueden ser duros como el diamante o blandos como el azufre. Al contrario de los metales, son muy frágiles y no pueden estirarse en hilos ni en láminas. Se encuentran en los tres estados de la materia a temperatura ambiente: son gases (como el oxígeno), líquidos (bromo) y sólidos (como el carbono). No tienen brillo metálico y no reflejan la luz. Muchos no metales se encuentran en todos los seres vivos: carbono, hidrógeno, oxígeno, nitrógeno, fósforo y azufre en cantidades importantes. Otros son oligoelementos: flúor, silicio, arsénico, yodo, cloro.
ENLACE QUIMICO DE OXIDOS METALICOS...
Enlaces químicos
La unión de 2 o más átomos
energía
Características longitud determinar la estructura de la molécula en el espacio
Del enlace
Ángulo
Energía de enlace: es la misma energía posible que mantiene a los átomos unidos para lograr su estabilidad
Longitud de enlace: Es la distancia intermolecular entre átomos
La electronegatividad aumenta de derecha a izquierda
Ángulo de enlace: Es el ángulo que forma los diferentes átomos con respecto al átomo central ( el átomo más electronegativo será el átomo central
Orbital atómico: Región en el espacio donde la probabilidad de encontrar un electrón es máxima
Ionico: se lleva a cabo entre elementos muy electronegativos y elementos electropositivos
Covalente:
La unión de 2 o más átomos
energía
Características longitud determinar la estructura de la molécula en el espacio
Del enlace
Ángulo
Energía de enlace: es la misma energía posible que mantiene a los átomos unidos para lograr su estabilidad
Longitud de enlace: Es la distancia intermolecular entre átomos
La electronegatividad aumenta de derecha a izquierda
Ángulo de enlace: Es el ángulo que forma los diferentes átomos con respecto al átomo central ( el átomo más electronegativo será el átomo central
Orbital atómico: Región en el espacio donde la probabilidad de encontrar un electrón es máxima
Enlaces Químicos
Ionico: se lleva a cabo entre elementos muy electronegativos y elementos electropositivos
Covalente:
- Polar
- No polar
- Coordinado
REPRESENTACIOND E LEWIS
La Estructura de Lewis, o puede ser llamada diagrama de punto, modelo de Lewis o representación de Lewis, es una representación gráfica que muestra los enlaces entre los átomos de una molécula y los pares de electrones solitarios que puedan existir. Diagrama de Lewis se puede usar tanto para representar moléculas formadas por la unión de sus átomos mediante enlace covalente como complejos de coordinación. La estructura de Lewis fue propuesta por Gilbert Lewis, quien lo introdujo por primera vez en 1915 en su artículo La molécula y el átomo.
Las estructuras de Lewis muestran los diferentes átomos de una determinada molécula usando su símbolo químico y líneas que se trazan entre los átomos que se unen entre sí. En ocasiones, para representar cada enlace, se usan pares de puntos en vez de líneas. Los electrones desapartados (los que no participan en los enlaces) se representan mediante una línea o con un par de puntos, y se colocan alrededor de los átomos a los que pertenece.
Las estructuras de Lewis muestran los diferentes átomos de una determinada molécula usando su símbolo químico y líneas que se trazan entre los átomos que se unen entre sí. En ocasiones, para representar cada enlace, se usan pares de puntos en vez de líneas. Los electrones desapartados (los que no participan en los enlaces) se representan mediante una línea o con un par de puntos, y se colocan alrededor de los átomos a los que pertenece.
PROPIEDADES PERIODICAS
Una de las ventajas de la Tabla Periódica es que permite predecir las propiedades de los elementos con sólo ver su posición dentro de ella. Además se debe mencionar que la tabla periódica permite realizar comparaciones entre diferentes propiedades de los elementos. Estas propiedades se conocen como PROPIEDADES PERIÓDICAS. Las principales propiedades periódicas son: volumen atómico, potencial de ionización, afinidad electrónica y electronegatividad.
Radio Atómico.
El Radio atómico que es una medida del tamaño atómico decrece a lo largo de un período y aumenta al ir bajando de período (Niveles superiores). La explicación de ésto es que el núcleo va aumentando de carga para un mismo período por lo que los electrones son más fuertemente atraídos hacia el núcleo. El radio atómico aumenta al añadir un nuevo nivel de energía.
La distancia de los electrones más externos al núcleo. Esta distancia se mide
en Angström (A=10-8), dentro de un grupo Sistema periódico, a medida que aumenta el número atómico de los miembros de una familia aumenta la densidad, ya que la masa atómica crece mas que el volumen atómico, el color F (gas amarillo verdoso), Cl (gas verde),
Br (líquido rojo), I sólido (negro púrpura), el lumen y el radio atómico, el carácter metálico, el radio iónico, aunque el radio iónico de los elementos metálicos es menor que su radio atómico.
Energía de Ionización
Se conoce como primera energía de ionización a la energía necesaria para separar el electrón más externo de un átomo neutro en estado gaseoso sin proporcionarle energía cinética.
Según esta definición, E.I. dependerá de tres factores: la distancia del electrón al núcleo, la carga nuclear y el efecto pantalla.
Emplea el método de Slater para calcular las afinidades electrónicas de los elementos del segundo período y compara sus resultados con los experimentales de la tabla 9.5 del Cruz,Chamizo & Garritz (Mr. Profe & Jefe). ¿Qué puedes comentar al respecto?
La variación de la energía de ionización se explica a continuación:
Dentro de un mismo grupo la E.I. disminuye de arriba a abajo. Esto se debe a que conforme descendemos en la tabla periódica los átomos tienen más electrones, lo cual disminuye la atracción sobre el electrón más externo (efecto pantalla).
En un mismo periodo la E.I. aumenta de izquierda a derecha. Este comportamiento se explica debido a que conforme avanzamos de izquierda a derecha, el electrón externo del átomo está menos alejado del núcleo y por tanto la fuerza con la cual es atrído aumenta. (distancia al núcleo, radio atómico).
Una regla empírica que relaciona en forma aproximada los valores de
altas energías de ionización sucesivas de electrones que ocupan la misma capa atómica es In = (n+1)/n * I(n-1) Utilizando el dato experimental de I3, estima con ella el valor de I4 para estaño, antimonio, telurio y yodo, y discute su validez.
El Radio atómico que es una medida del tamaño atómico decrece a lo largo de un período y aumenta al ir bajando de período (Niveles superiores). La explicación de ésto es que el núcleo va aumentando de carga para un mismo período por lo que los electrones son más fuertemente atraídos hacia el núcleo. El radio atómico aumenta al añadir un nuevo nivel de energía.
La distancia de los electrones más externos al núcleo. Esta distancia se mide
en Angström (A=10-8), dentro de un grupo Sistema periódico, a medida que aumenta el número atómico de los miembros de una familia aumenta la densidad, ya que la masa atómica crece mas que el volumen atómico, el color F (gas amarillo verdoso), Cl (gas verde),
Br (líquido rojo), I sólido (negro púrpura), el lumen y el radio atómico, el carácter metálico, el radio iónico, aunque el radio iónico de los elementos metálicos es menor que su radio atómico.
Se conoce como primera energía de ionización a la energía necesaria para separar el electrón más externo de un átomo neutro en estado gaseoso sin proporcionarle energía cinética.
Según esta definición, E.I. dependerá de tres factores: la distancia del electrón al núcleo, la carga nuclear y el efecto pantalla.
Emplea el método de Slater para calcular las afinidades electrónicas de los elementos del segundo período y compara sus resultados con los experimentales de la tabla 9.5 del Cruz,Chamizo & Garritz (Mr. Profe & Jefe). ¿Qué puedes comentar al respecto?
La variación de la energía de ionización se explica a continuación:
Dentro de un mismo grupo la E.I. disminuye de arriba a abajo. Esto se debe a que conforme descendemos en la tabla periódica los átomos tienen más electrones, lo cual disminuye la atracción sobre el electrón más externo (efecto pantalla).
En un mismo periodo la E.I. aumenta de izquierda a derecha. Este comportamiento se explica debido a que conforme avanzamos de izquierda a derecha, el electrón externo del átomo está menos alejado del núcleo y por tanto la fuerza con la cual es atrído aumenta. (distancia al núcleo, radio atómico).
Una regla empírica que relaciona en forma aproximada los valores de
altas energías de ionización sucesivas de electrones que ocupan la misma capa atómica es In = (n+1)/n * I(n-1) Utilizando el dato experimental de I3, estima con ella el valor de I4 para estaño, antimonio, telurio y yodo, y discute su validez.
ESTRUCTURA ATOMICA
La experiencia de Rutherford fue crucial en la determinación de la estructura atómica. Los párrafos que siguen son un extracto de su propia comunicación (1911):
"Es un hecho bien conocido que las partículas alfa y beta sufren desviaciones de sus trayectorias rectilíneas a causa de las interacciones con los átomos de la materia.
Parece indudable que estas partículas de movimiento veloz pasan en su recorrido a través de los átomos, y las desviaciones observadas son debidas al campo eléctrico dentro del sistema atómico.
Las observaciones de Geiger y Mardsen sobre la dispersión de partículas alfa, indican que algunas de estas partículas deben de experimentar en un solo encuentro desviaciones superiores a un ángulo recto.
Un cálculo simple demuestra que el átomo debe de ser asiento de un intenso campo eléctrico para que se produzca una gran desviación en una colisión simple..."
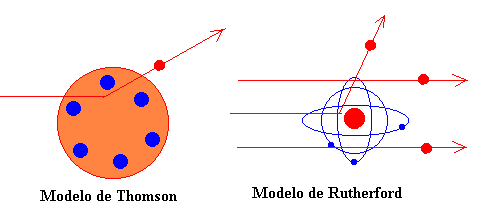
En aquella época Thomson había elaborado un modelo de átomo consistente en un cierto número N de corpúsculos cargados negativamente, acompañados de una cantidad igual de electricidad positiva distribuida uniformemente en toda una esfera. Rutherford pone a prueba este modelo y sugiere el actual modelo de átomo.
"La teoría de Thomson está basada en la hipótesis de que la dispersión debida a un simple choque atómico es pequeña y que la estructura supuesta para el átomo no admite una desviación muy grande de una partícula alfa que incida sobre el mismo, a menos que se suponga que el diámetro de la esfera de electricidad positiva es pequeño en comparación con el diámetro de influencia del átomo. Puesto que las partículas alfa y beta atraviesan el átomo, un estudio riguroso de la naturaleza de la desviación debe proporcionar cierta luz sobre la constitución del átomo, capaz de producir los efectos observados. En efecto, la dispersión de partículas cargadas de alta velocidad por los átomos de la materia constituyen uno de los métodos más prometedores de ataque del problema.."
En la simulación de la experiencia de Rutherford, consideramos una muestra de un determinado material a elegir entre varios y la situamos en el centro de un conjunto de detectores dispuestos a su alrededor. El blanco es bombardeado por partículas alfa de cierta energía producidas por un material radioactivo. Se observa que muy pocas partículas son desviadas un ángulo apreciable, y se producen muy raramente sucesos en los que la partícula alfa retrocede.
Se denomina parámetro de impacto a la distancia existente entre la dirección de la partícula incidente y el centro de fuerzas.
Una vez que la partícula ha sido dispersada por el núcleo se aleja del centro de fuerzas siguiendo una trayectoria que tiende asintóticamente a una línea recta. El ángulo F que forma dicha recta con el eje horizontal se denomina ángulo de dispersión.
La fórmula que relaciona el parámetro de impacto b con el ángulo de dispersión F para una energía E dada de la partícula alfa, como hemos visto, es la siguiente.
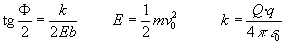
"Es un hecho bien conocido que las partículas alfa y beta sufren desviaciones de sus trayectorias rectilíneas a causa de las interacciones con los átomos de la materia.
Parece indudable que estas partículas de movimiento veloz pasan en su recorrido a través de los átomos, y las desviaciones observadas son debidas al campo eléctrico dentro del sistema atómico.
Las observaciones de Geiger y Mardsen sobre la dispersión de partículas alfa, indican que algunas de estas partículas deben de experimentar en un solo encuentro desviaciones superiores a un ángulo recto.
Un cálculo simple demuestra que el átomo debe de ser asiento de un intenso campo eléctrico para que se produzca una gran desviación en una colisión simple..."

En aquella época Thomson había elaborado un modelo de átomo consistente en un cierto número N de corpúsculos cargados negativamente, acompañados de una cantidad igual de electricidad positiva distribuida uniformemente en toda una esfera. Rutherford pone a prueba este modelo y sugiere el actual modelo de átomo.
"La teoría de Thomson está basada en la hipótesis de que la dispersión debida a un simple choque atómico es pequeña y que la estructura supuesta para el átomo no admite una desviación muy grande de una partícula alfa que incida sobre el mismo, a menos que se suponga que el diámetro de la esfera de electricidad positiva es pequeño en comparación con el diámetro de influencia del átomo. Puesto que las partículas alfa y beta atraviesan el átomo, un estudio riguroso de la naturaleza de la desviación debe proporcionar cierta luz sobre la constitución del átomo, capaz de producir los efectos observados. En efecto, la dispersión de partículas cargadas de alta velocidad por los átomos de la materia constituyen uno de los métodos más prometedores de ataque del problema.."
En la simulación de la experiencia de Rutherford, consideramos una muestra de un determinado material a elegir entre varios y la situamos en el centro de un conjunto de detectores dispuestos a su alrededor. El blanco es bombardeado por partículas alfa de cierta energía producidas por un material radioactivo. Se observa que muy pocas partículas son desviadas un ángulo apreciable, y se producen muy raramente sucesos en los que la partícula alfa retrocede.
Descripción
Como hemos visto al estudiar el fenómeno de la dispersión, la interacción entre partículas cargadas positivamente corresponde a una fuerza central y conservativa. La energía total es siempre positiva por lo que la trayectoria es siempre una hipérbola.Se denomina parámetro de impacto a la distancia existente entre la dirección de la partícula incidente y el centro de fuerzas.
Una vez que la partícula ha sido dispersada por el núcleo se aleja del centro de fuerzas siguiendo una trayectoria que tiende asintóticamente a una línea recta. El ángulo F que forma dicha recta con el eje horizontal se denomina ángulo de dispersión.
La fórmula que relaciona el parámetro de impacto b con el ángulo de dispersión F para una energía E dada de la partícula alfa, como hemos visto, es la siguiente.
REACCION QUIMICA DEL OXIGENO CON METALES Y NO METALES...
El oxígeno gaseoso se condensa formando un líquido azul pálido fuertemente magnético. El oxígeno sólido de color azul pálido se obtiene comprimiendo el líquido. La masa atómica del oxígeno es 15,9994; a la presión atmosférica, el elemento tiene un punto de ebullición de -182,96 °C, un punto de fusión de -218.4 °C y una densidad de 1,429 g/l a 0 °C.
El oxígeno constituye el 21% en volumen o el 23,15% en masa de la atmósfera, el 85,8% en masa de los océanos (el agua pura contiene un 88,8% de oxígeno), el 46,7% en masa de la corteza terrestre (como componente de la mayoría de las rocas y minerales). El oxígeno representa un 60% del cuerpo humano. Se encuentra en todos los tejidos vivos. Casi todas las plantas y animales, incluyendo los seres humanos, requieren oxígeno, ya sea en estado libre o combinado, para mantenerse con vida. Véase Respiración.
Se conocen tres formas estructurales del oxígeno: el oxígeno ordinario, que contiene dos átomos por molécula y cuya fórmula es O2; el ozono, que contiene tres átomos por molécula y cuya fórmula es O3, y una forma no magnética azul pálida, el O4, que contiene cuatro átomos por molécula, y se descompone fácilmente en oxígeno ordinario. Se conocen tres isótopos estables del oxígeno: el oxígeno 16 (de masa atómica 16) es el más abundante. Representa un 99,76% del oxígeno ordinario y se utilizó en la determinación de las masas atómicas hasta la década de 1960 (véase Átomo).
El oxígeno se prepara en el laboratorio a partir de ciertas sales como el clorato de potasio, el peróxido de bario y el peróxido de sodio. Los métodos industriales más importantes para la obtención de oxígeno son la electrólisis del agua y la destilación fraccionada de aire líquido. En este último método, se licúa el aire y se deja evaporar. En el aire líquido, el nitrógeno es más volátil y se evapora antes, quedando el oxígeno en estado líquido. A continuación el oxígeno se almacena y se transporta en forma líquida o gaseosa.
El oxígeno está presente en muchos compuestos orgánicos e inorgánicos. Forma compuestos llamados óxidos con casi todos los elementos, incluyendo algunos de los gases nobles. La reacción química en la cual se forma el óxido se llama oxidación. La velocidad de la reacción varía según los elementos. La combustión ordinaria es una forma de oxidación muy rápida. En la combustión espontánea, el calor desarrollado por la reacción de oxidación es suficientemente grande para elevar la temperatura de la sustancia hasta el punto de producir llamas. Por ejemplo, el fósforo combina tan vigorosamente con el oxígeno, que el calor liberado en la reacción hace que el fósforo se funda y arda. Algunas sustancias finamente divididas presentan un área tan grande de superficie al aire, que arden formando llamas por combustión espontánea; a éstas se las llama sustancias pirofóricas. El azufre, el hidrógeno, el sodio y el magnesio combinan con el oxígeno menos energéticamente y sólo arden después de la ignición. Algunos elementos como el cobre y el mercurio reaccionan lentamente para formar los óxidos, incluso cuando se les calienta. Los metales inertes, como el platino, el iridio y el oro únicamente forman óxidos por métodos indirectos. (Para mayor información sobre los óxidos, ver los artículos correspondientes a cada elemento).
contaminacion ambiental
La contaminación es cualquier sustancia o forma de energía que puede provocar algún daño o desequilibrio (irreversible o no) en un ecosistema, en el medio físico o en un ser vivo. Es siempre una alteración negativa del estado natural del medio ambiente, y por tanto, se genera como consecuencia de la actividad humana.
Para que exista contaminación, la sustancia contaminante deberá estar en cantidad relativa suficiente como para provocar ese desequilibrio. Esta cantidad relativa puede expresarse como la masa de la sustancia introducida en relación con la masa o el volumen del medio receptor de la misma. Este cociente recibe el nombre de concentración.
Los agentes contaminantes tienen relación con el crecimiento de la población y el consumo (combustibles fósiles, la generación de basura, desechos industriales, etc.), ya que, al aumentar estos, la contaminación que ocasionan es mayor.
Por su consistencia, los contaminantes se clasifican en sólidos, líquidos y gaseosos. Se descartan los generados por procesos naturales, ya que, por definición, no contaminan.
Los agentes sólidos están constituidos por la basura en sus diversas presentaciones. Provocan contaminación del suelo, del aire y del agua. Del suelo porque produce microorganismos y animales dañinos; del aire porque produce mal olor y gases tóxicos, y del agua porque la ensucia y no puede utilizarse.
Los agentes líquidos incluyen las aguas negras, los desechos industriales, los derrames de combustibles derivados del petróleo, los cuales dañan básicamente el agua de ríos, lagos, mares y océanos, y con ello provocan la muerte de diversas especies.
Los agentes gaseosos incluyen la combustión del petróleo (óxido de nitrógeno y azufre) y la quema de combustibles como la gasolina (que libera monóxido de carbono), la basura y los desechos de plantas y animales.
Todos los agentes contaminantes provienen de una fuente determinada y pueden provocar enfermedades respiratorias y digestivas. Es necesario que la sociedad humana tome conciencia del problema.
Se denomina contaminación atmosférica o contaminación ambiental a la presencia en el ambiente de cualquier agente (físico, químico o biológico) o bien de una combinación de varios agentes en lugares, formas y concentraciones tales que sean o puedan ser nocivos para la salud, para la seguridad o para el bienestar de la población, o que puedan ser perjudiciales para la vida vegetal o animal, o que impidan el uso habitual de las propiedades y lugares de recreación y el goce de los mismos. La contaminación ambiental es también la incorporación a los cuerpos receptores de sustancias sólidas, líquidas o gaseosas o de mezclas de ellas, siempre que alteren desfavorablemente las condiciones naturales de los mismos o que puedan afectar la salud, la higiene o el bienestar del público.
Para que exista contaminación, la sustancia contaminante deberá estar en cantidad relativa suficiente como para provocar ese desequilibrio. Esta cantidad relativa puede expresarse como la masa de la sustancia introducida en relación con la masa o el volumen del medio receptor de la misma. Este cociente recibe el nombre de concentración.
Los agentes contaminantes tienen relación con el crecimiento de la población y el consumo (combustibles fósiles, la generación de basura, desechos industriales, etc.), ya que, al aumentar estos, la contaminación que ocasionan es mayor.
Por su consistencia, los contaminantes se clasifican en sólidos, líquidos y gaseosos. Se descartan los generados por procesos naturales, ya que, por definición, no contaminan.
Los agentes sólidos están constituidos por la basura en sus diversas presentaciones. Provocan contaminación del suelo, del aire y del agua. Del suelo porque produce microorganismos y animales dañinos; del aire porque produce mal olor y gases tóxicos, y del agua porque la ensucia y no puede utilizarse.
Los agentes líquidos incluyen las aguas negras, los desechos industriales, los derrames de combustibles derivados del petróleo, los cuales dañan básicamente el agua de ríos, lagos, mares y océanos, y con ello provocan la muerte de diversas especies.
Los agentes gaseosos incluyen la combustión del petróleo (óxido de nitrógeno y azufre) y la quema de combustibles como la gasolina (que libera monóxido de carbono), la basura y los desechos de plantas y animales.
Todos los agentes contaminantes provienen de una fuente determinada y pueden provocar enfermedades respiratorias y digestivas. Es necesario que la sociedad humana tome conciencia del problema.
Se denomina contaminación atmosférica o contaminación ambiental a la presencia en el ambiente de cualquier agente (físico, químico o biológico) o bien de una combinación de varios agentes en lugares, formas y concentraciones tales que sean o puedan ser nocivos para la salud, para la seguridad o para el bienestar de la población, o que puedan ser perjudiciales para la vida vegetal o animal, o que impidan el uso habitual de las propiedades y lugares de recreación y el goce de los mismos. La contaminación ambiental es también la incorporación a los cuerpos receptores de sustancias sólidas, líquidas o gaseosas o de mezclas de ellas, siempre que alteren desfavorablemente las condiciones naturales de los mismos o que puedan afectar la salud, la higiene o el bienestar del público.
efecto invernadero
Se denomina efecto invernadero al fenómeno por el cual determinados gases, que son componentes de la atmósfera planetaria, retienen parte de la energía que el suelo emite por haber sido calentado por la radiación solar. Afecta a todos los cuerpos planetarios dotados de atmósfera. De acuerdo con la mayoría de la comunidad científica, el efecto invernadero se está viendo acentuado en la Tierra por la emisión de ciertos gases, como el dióxido de carbono y el metano, debido a la actividad humana.
Este fenómeno evita que la energía solar recibida constantemente por la Tierra vuelva inmediatamente al espacio, produciendo a escala planetaria un efecto similar al observado en un invernadero.
Este fenómeno evita que la energía solar recibida constantemente por la Tierra vuelva inmediatamente al espacio, produciendo a escala planetaria un efecto similar al observado en un invernadero.
combustion
La combustión es una reacción química en la cual generalmente se desprende una gran cantidad de calor y luz.
En toda combustión existe un elemento que arde y se denomina (combustible) y otro que produce la combustión (comburente), generalmente oxígeno en forma de O2 gaseoso. Los explosivos tienen oxígeno ligado químicamente por lo que no necesitan el oxígeno del aire para realizar la combustión.
Los tipos más frecuentes de combustible son los materiales orgánicos que contienen carbono e hidrógeno. En una reacción completa todos los elementos tienen el mayor estado de oxidación. Los productos que se forman son el dióxido de carbono (CO2) y el agua, el dióxido de azufre (SO2) (si el combustible contiene azufre) y pueden aparecer óxidos de nitrógeno (NOx), dependiendo de la temperatura de reacción.
En la combustión incompleta los productos que se queman pueden no reaccionar con el mayor estado de oxidación, debido a que el comburente y el combustible no están en la proporción adecuada, dando como resultado compuestos como el monóxido de carbono (CO). Además, pueden generarse cenizas.
El proceso de destruir materiales por combustión se conoce como incineración.
Para iniciar la combustión de cualquier combustible, es necesario alcanzar una temperatura mínima, llamada temperatura de ignición, que se define como, en °C y a 1 atm, temperatura a la que los vapores de un combustible arden espontáneamente.
La temperatura de inflamación, en °C y a 1 atm es aquella que, una vez encendidos los vapores del combustible, éstos continúan por si mismos el proceso de combustión.
En toda combustión existe un elemento que arde y se denomina (combustible) y otro que produce la combustión (comburente), generalmente oxígeno en forma de O2 gaseoso. Los explosivos tienen oxígeno ligado químicamente por lo que no necesitan el oxígeno del aire para realizar la combustión.
Los tipos más frecuentes de combustible son los materiales orgánicos que contienen carbono e hidrógeno. En una reacción completa todos los elementos tienen el mayor estado de oxidación. Los productos que se forman son el dióxido de carbono (CO2) y el agua, el dióxido de azufre (SO2) (si el combustible contiene azufre) y pueden aparecer óxidos de nitrógeno (NOx), dependiendo de la temperatura de reacción.
En la combustión incompleta los productos que se queman pueden no reaccionar con el mayor estado de oxidación, debido a que el comburente y el combustible no están en la proporción adecuada, dando como resultado compuestos como el monóxido de carbono (CO). Además, pueden generarse cenizas.
El proceso de destruir materiales por combustión se conoce como incineración.
Para iniciar la combustión de cualquier combustible, es necesario alcanzar una temperatura mínima, llamada temperatura de ignición, que se define como, en °C y a 1 atm, temperatura a la que los vapores de un combustible arden espontáneamente.
La temperatura de inflamación, en °C y a 1 atm es aquella que, una vez encendidos los vapores del combustible, éstos continúan por si mismos el proceso de combustión.
martes, 16 de noviembre de 2010
LEWIS
¿Que son y cómo se representan los electrones de valencia?
Los electrones de valencia son los electrones que se encuentran ubicados en la última capa o nivel energético de determinado átomo. Se llaman así porque estos determinan la valencia o número de oxidación de determinado elemento.
Escribir la estructura de Lewis de cada Familia
| Equipo | Grupo y Familia | Estructura de Lewis de los elementos químicos |
| 1 | I alcalinos | H*, Li*, Na*,K*,Rb*,Cs*,Fr,* |
| 2 | II alcalinotérreos. | *Be*, *Mg*,*Ca*,*Sr*, *Ba*,*Ra* |
| 3 | III térreos | * * * * * * B* *Al* *Ga* *In* *Tl* |
| 4 | IV carbono | + + + + + +C+, +Si+, +Ge+, +Sn+, +Pb+ + + + + + |
| 5 | V nitrogenoides | * * * * * *N* ,*P*,*As*,*Sb*,*Bi* ** ** ** ** ** |
| 6 | VI los carbógenos o anfígenos | ** ** ** ** ** **O** , **S**,** Se** ,**Te** ,**Po**, |
| 7 | VII los halógenos | ** ** ** ** ** **F** **Cl** **Br** **I** **At+** * * * * * |
| 8 | VIII gases nobles | ** ** ** ** ** *He* **Ne** **Ar** **Kr** **Xe** **Rn** ** ** ** ** ** |
· En química, el enlace iónico es una unión que resulta de la presencia de fuerza de atracción electrostática entre los iones de distinto signo, es decir, uno fuertemente electropositivo (baja energía de ionización) y otro fuertemente electronegativo (alta afinidad electrónica). Eso se da cuando en el enlace, uno de los átomos capta electrones del otro.
· Un enlace covalente se produce por compartición de electrones entre dos átomos. Este tipo de enlace se produce cuando existe electronegatividad polar pero la diferencia de electronegatividades entre los átomos no es suficientemente grande como para que se efectúe transferencia de electrones. De esta forma, los dos átomos comparten uno o más pares electrónicos en un nuevo tipo de orbital, denominado orbital molecular. Los enlaces covalentes se suelen producir entre elementos gaseosos no metales.
· En un enlace metálico, los electrones de enlace están des localizados en una estructura de átomos. En contraste, en los compuestos iónicos, la ubicación de los electrones enlazantes y sus cargas es estática. Debido a la deslocalización o el libre movimiento de los electrones, se tienen las propiedades metálicas de conductividad, ductilidad y dureza.
Determinación del tipo de enlace químico:
· Material: Probador de conductividad eléctrica, capsula de porcelana.
· Sustancias: Cloruro de sodio, sacarosa, metales, agua, alcohol.
· Procedimiento:
· a.- Colocar en la capsula de porcelana una muestra del cloruro de sodio, probar su conductividad eléctrica en seco, agregar unas gotas de agua y probar nuevamente su conductividad eléctrica. Anotar las observaciones.
· b.- Repetir el paso a con las demás sustancias.
· Observaciones:
| Sustancia | Conductividad en seco | Conductividad en húmedo | Tipo de enlace químico |
| Cloruro de sodio | No tiene conductividad | Si hay conductividad | Iónico |
| Sacarosa | No presenta conductividad | Presenta poca conductividad | Covalente |
| Metal | Si hay conductividad | Si presenta conductividad | Metálico |
| Alcohol | No hay conductividad | Poca conductividad | |
| Agua | No hay conductividad | Si hay conductividad. | Covalente |
· Conclusiones:
Con los experimentos realizados vimos los diferentes tipos de enlaces que hay como son el iónico al prestar uno de sus electrones para formar la capa de valencia, el covalente compartir los electrones y el metálico es la nube electrónica que permite el paso de la corriente eléctrica.
miércoles, 10 de noviembre de 2010
SEMANA14
¿Cuales son las propiedades periódicas de los elementos químicos?
- .
- .
- El carácter metálico y no metálico.
| Equipo | Propiedades periódicas de los elementos. |
| 1 | La configuración electrónica La configuración electrónica del átomo de un elemento corresponde a la ubicación de los electrones en los orbitales de los diferentes niveles de energía. La manera de mostrar cómo se distribuyen los electrones en un átomo, es a través de la configuración electrónica. El orden en el que se van llenando los niveles de energía es: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p. |
| 2 | La energía de ionización.- La energía de ionización, potencial de ionización o EI es la energía necesaria para arrancar un electrón de un átomo perteneciente a una sustancia que se encuentra en estado gaseoso.[1] La reacción puede expresarse de la siguiente forma: Siendo A(g) los átomos neutros de una sustancia elemental en estado gaseoso; EI, la energía de ionización y |
| 3 | La afinidad electrónica. se define como la energía involucrada cuando un átomo gaseoso neutro en su estado fundamental (de mínima energía) captura un electrón y forma un ion mononegativo: La electroafinidad aumenta cuando el tamaño del átomo disminuye, el efecto pantalla aumenta y cuando el nº atómico disminuye. Visto de otra manera: aumenta de izquierda a derecha, y de abajo hacia arriba, al igual que lo hace la electronegatividad |
| 4 | La electronegatividad.
los electrones, o densidad electrónica, cuando forma un enlace covalente en una molécula.[1] |
| 5 | El volumen atómico.- es el volumen que ocupa un mol de átomo del elemento considerado. Se obtiene según la siguiente fórmula: Vol atom = masa atómica / densidad. Se mide en unidades de volumen por mol, por ejemplo, cc/mol. |
| 6 | El número de oxidación. Las reglas para los números de oxidación pueden deducirse si se tiene en cuenta lo dicho con respecto a que los elementos, al unirse, pierden, ganan o comparten electrones para llegar a una estructura más estable. Los números de oxidación son consecuencia de esto. |
Suscribirse a:
Entradas (Atom)

